Alzheimer et Démences
Publié le 07 aoû 2011Lecture 10 min
Diagnostic des démences de type Alzheimer : TDM, IRM, TEMP ou TEP ? À quand la technique de neuro-imagerie (quasi) idéale ?
P. TELLIER*, I.-L. DELBARRE**, P. Le COZ** *Centre de Médecine Nucléaire de l’Artois, Arras **LDBmédias, Paris ***Service de Neurologie, Centre hospitalier d’Arras
Les démences de type Alzheimer (DTA) sont les plus fréquents des processus neurodégénératifs affectant le système nerveux central. Les troubles de la mémoire sont au centre de la sémiologie des DTA dès le stade du déclin cognitif léger (DCL), qui peut d’ailleurs précéder de longue date cette forme de démence. En l’espace d’une quinzaine d’années, les progrès des techniques de neuro-imagerie ont permis une approche diagnostique plus précise de la maladie, mais force est de reconnaître qu’aucun des examens actuellement disponibles n’offre la solution idéale. Cet état de fait n’interdit pas le développement de stratégies diagnostiques performantes, cependant variables d’un pays à l’autre en fonction des indications validées par des organismes tels la FDA (Food and Drug Administration), la Haute Autorité de santé (HAS) ou encore l’Agence européenne du médicament. L’IRM fonctionnelle qui est un outil extraordinaire en neurophysiologie ne sera pas abordée ici, car elle n’a actuellement aucune application dans la pratique neurologique courante.
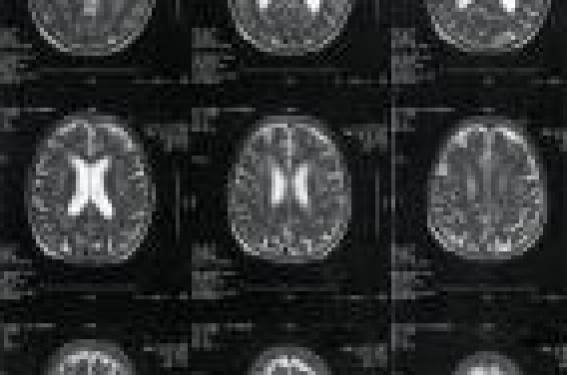
Neuro-imagerie structurale ou fonctionnelle : généralités La neuro-imagerie structurale ou fonctionnelle, dite encore moléculaire, regroupe l’ensemble des techniques d’imagerie visant à explorer les structures anatomiques et/ou le métabolisme du cerveau, au demeurant étroitement couplé à sa perfusion pour des raisons d’efficience physiologique. Les examens qui donnent en priorité accès aux structures cérébrales sont principalement la tomodensitométrie (TDM) et l’imagerie par résonance magnétique (IRM). Figure 1. IRM encéphalique (coupes axiales) : mise en évidence de nombreux hypersignaux de la substance blanche chez un patient âgé atteint d’une démence type Alzheimer. Ceux qui relèvent plutôt de l’imagerie dite fonctionnelle ou métabolique sont la tomoscintigraphie d’émission monophotonique (TEMP) et la tomoscintigraphie par émission de positons (TEP). Pour ces deux explorations fonctionnelles, il faut injecter par voie intraveineuse le radiopharmaceutique approprié. En l’occurrence, dans le cas de la TEMP, il s’agit d’un traceur de la perfusion cérébrale, soit le HMPAO (Hexaméthylpropylène- amine oxime) soit l’ECD (éthyl-cystéinate dimer) tous deux marqués par le technétium 99m qui est un émetteur monophotonique, l’énergie du rayonnement étant de 140 keV. Les appareils destinés à l’acquisition des données sont des gamma-caméras tomographiques conventionnelles. Dans le cas de la TEP, c’est actuellement le 18fluorodéoxyglucose (18FDG), un analogue du glucose qui est administré, le 18F étant un émetteur de positons. Après interaction avec un électron négatif tissulaire, ces derniers donnent naissance à deux photons d’annihilation de 511 keV chacun, diamétralement opposés. En TEP, l’acquisition des données repose sur les caméras à positons, en sachant qu’à l’heure actuelle, dans certains pays industrialisés dont la France, l’indication de la 18FDGTEP dans le bilan des démences n’est pas encore validée. Cette situation va évoluer, car d’ici peu, d’autres radiopharmaceutiques vont être mis sur le marché : il s’agit en particulier des l igands des plaques amyloïdes, notamment le PIB (Pittsburgh compound B), marqué par le carbone 11 ou le fluor 18, tous deux émetteurs de positons. Quelle que soit la technique utilisée, l’objectif est de détecter les lésions anatomiques ou les anomalies fonctionnelles plus ou moins caractéristiques des DTA, idéalement à leur phase précoce qui prend volontiers l’apparence clinique d’un déficit cognitif léger (DCL). Il faudrait disposer en fait des outils qui permettraient d’évaluer le risque de DTA face à un DCL, ce qui n’est pas encore le cas. Apport de l’imagerie structurale dans les DTA Dans les recommandations de la HAS et d’autres organismes apparentés, l’imagerie structurale doit être prescrite en première intention face à une suspicion de démence, y compris les DTA. Figure 2. TEMP encéphalique normale (coupes axiales). Radiopharmaceutique : ECD marqué par le technétium 99m (99m Tc-ECD). L’objectif de la TDM et de l’IRM est ici, en priorité, la recherche d’une maladie neurologique potentiellement curable, qu’il s’agisse d’une lésion expansive ou d’une hydrocéphalie communicante à pression normale. Au passage, ces explorations sont douées d’une haute résolution spatiale de l’ordre du millimètre, de sorte qu’elles peuvent identifier des anomalies structurales plaidant en faveur d’une DTA. Certes, la TDM est relativement peu onéreuse et largement accessible. Cependant, en pratique courante, le neurologue tend à privilégier l’IRM face à un DCL patent ou à une suspicion de DTA. L’interprétation de l’IRM est souvent visuelle et par essence subjective, alors qu’il existe des logiciels capables de mesurer les volumes régionaux et d’objectiver ainsi une atrophie de l’hippocampe ou de la partie mésiale du lobe temporal. Cette IRM dite volumétrique est séduisante, mais relativement lourde à mettre en oeuvre. La méthode dite VBM (Voxel-based morphometry) est plus précise et moins lourde, mais elle suppose de disposer d’un logiciel sophistiqué et onéreux. En outre, les anomalies structurales détectées par l’IRM ne sont pas spécifiques des DTA, car elles peuvent s’observer dans d’autres démences. Leur progression est en règle parallèle à l’évolution clinique de la maladie. En cas de DCL, l’atrophie progressive du cortex entorhinal et de l’hippocampe est associée à une augmentation du risque de DTA. L’IRM peut également mettre en évidence des hypersignaux de la substance blanche non spécifiques a priori, mais il peut en être autrement si ces anomalies sont à la fois étendues et évolutives (figure 1). Figure 3. TEMP encéphalique anormale (coupes axiales). Radiopharmaceutique : 99m Tc-ECD. Mise en évidence d’un déficit limité de la perfusion cérébrale au niveau de la région temporo-occipitale gauche chez un patient âgé atteint d’un DCL. Même dans ce cas de figure, elles ne sont pas spécifiques des DTA, alors qu’elles sont associées à une majoration parfois rapide des troubles cognitifs du sujet âgé. L’imagerie par tenseur de diffusion, encore appelée IRM de diffusion, serait plus sensible dans la détection d’anomalies plus fréquentes de la substance blanche temporale en cas de DTA. Ses performances diagnostiques seraient accrues si l’on ajoute l’atrophie de l’hippocampe aux perturbations de la diffusion tissulaire de l’eau. La contribution en pratique courante de l’IRM de diffusion reste cependant modeste, tout au moins dans le domaine des DTA. Apport de la tomoscintigraphie d’émission monophotonique (TEMP) Avec les radiotraceurs technétiés précédemment évoqués, respectivement le HMPAO et l’ECD, c’est la perfusion cérébrale qui est explorée, en sachant que cette dernière est étroi tement couplée au métabolisme. De ce fait, l’examen peut mettre en évidence des anomalies fonctionnelles qui orientent le diagnostic étiologique des démences et l’évaluation pronostique du DCL. La résolution spatiale de la TEMP est de l’ordre de 10 mm, de sorte que les images n’ont pas la précision anatomique de la TDM ou de l’IRM (figure 2). Leur qualité est cependant suffisante pour aboutir à des performances diagnostiques honorables par rapport à l’imagerie structurale ou encore à la 18F-FDG-TEP. Cet examen es t réal i sable en pratique courante depuis une vingtaine d’années. Figure 4. TEMP encéphalique anormale (coupe axiales). Radiopharmaceutique : 99m Tc-ECD. Mise en évidence de déficits étendus de la perfusion cérébrale au niveau du cortex hémisphérique droit en regard du carrefour temporopariéto-occipital, mais aussi du cortex frontopariétal. Petit déficit occipital gauche. Patient atteint d’une DTA évoluée associée à des lésions vasculaires. L’anomalie la plus fréquemment retrouvée, en cas de DTA ou de DCL, est un hypométabolisme du carrefour temporopariétooccipital et/ou du cortex temporopariétal dans sa portion mésiale (figure 3). Ces aires cérébrales font partie du cortex associatif postérieur. L’hypométabolisme s’étend au cortex frontopariétal quand la DTA s’aggrave (figure 4). Inversement, dans les formes débutantes ou encore en cas de DCL, ces anomalies sont souvent unilatérales, discrètes et localisées au cortex temporopariéto- occipital. Sans être pathognomiques, elles plaident en faveur d’une DTA, plutôt qu’en faveur d’une démence à corps de Lewy ou encore une démence fronto-temporale. La TEMP est également intéressante dans l’évaluation pronostique du DCL. L’interprétation des images est le plus souvent visuelle, mais elle peut aussi reposer sur une semi-quantification du type voxel par voxel au travers de logiciels comme le SPM (Statistical parametric mapping). Figure 5. 18F-FDG-TEP-TDM du corps entier normale, quadrant supérieur droit ; TEP encéphalique normale, quadrant inférieur droit : image de fusion TEP et TDM. La TEMP de perfusion cérébrale est appréciée des neurologues dans les centres de médecine nucléaire qui la pratiquent, quelle que soit la technique d’interprétation. La combinaison des données cliniques, des résultats de l’IRM et de la TEMP, et éventuellement des marqueurs dosés dans le LCR, permet de résoudre bon nombre de problèmes diagnostiques. Le développement de la TEP en neurologie pourrait aboutir à une redistribution des cartes à brève échéance, notamment en France. Apport de la tomoscintigraphie par émission de positons (TEP) La TEP-TDM suppose d’utiliser comme systèmes de détection, d’une part, une caméra à positons, d’autre part, un scanner spiralé. Cette technique d’imagerie fonctionnelle n’est utilisée en pratique courante qu’en oncologie dans un pays comme la France. Ailleurs, notamment aux États-Unis, elle est couramment indiquée dans le bilan des démences, y compris les DTA et le DCL, avec l’approbation de la FDA, mais aussi le remboursement de l’acte à la fois par Medicare et Medicaid, ceci depuis septembre 2004. Figure 6. TEP réalisée avec un marqueur des plaques amyloïdes, en l’occurrence le 18F-PIB (18F-flutemetamol). A (en haut) : coupes axiale et coronale. Patient âgé atteint d’une DTA. Mise en évidence d’une hyperfixation intense et étendue du radiotraceur au sein du cortex associatif postérieur. B (en bas) : mêmes coupes d’aspect normal chez un sujet âgé indemne de toute affection neurologique cliniquement patente. Absence de fixation significatif du 18F-flutemetamol. Le seul radiopharmaceutique utilisable dans ces indications est ici le 18F-FDG (figure 5). La sémiologie scintigraphique rejoint celle de la TEMP au travers d’un hypométabolisme touchant le cortex associatif postérieur, mais les images sont plus précises, car la résolution spatiale des caméras à positons est de l’ordre de 3 à 5 mm. Plusieurs études longitudinales ont démontré l’intérêt de la 18F-FDG dans les indications suivantes : • diagnostic positif des DTA ; • diagnostic différentiel entre les DTA et les autres démences ; • suivi du DCL avec évaluation du risque d’apparition d’une DTA. Voilà pour les explorations réalisées avec un analogue du glucose comme le 18F-FDG. D’autres radiopharmaceutiques sont en cours de développement, au stade d’étude de phase III. Il s’agit des marqueurs des plaques amyloïdes et/ou des dépôts neurofibrillaires, en l’occurrence le PIB, marqué par le carbone 11 ou le fluor 18 (figure 6). Ces marqueurs sont prometteurs, mais il leur reste à franchir l’évaluation clinique en cours. La période physique du carbone 11 est de 20 minutes, celle du fluor 18 de 2 heures. Le marquage au carbone 11 implique d’être à proximité d’un cyclotron, ce qui constitue un frein à la diffusion de la technique en pratique courante. D’autres ligands « moins avancés » visent les dysfonctionnements des voies de la neurotransmission centrale. Il est vrai que les processus biologiques sous-tendant les maladies neurodégénératives sont multiples et variés. La neuroimagerie du futur passe par ces étapes, mais il faut dans un premier temps qu’elle soit avalisée dans certains pays comme la France. Les caméras à positons sont désormais assez nombreuses, de sorte que la 18F-FDG-TEP devrait être utilisable en pratique courante dans l’exploration des maladies neurodégénératives.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :