Publié le 15 aoû 2011Lecture 14 min
Les diagnostics différentiels de la maladie d’Alzheimer en 2011
A. GABELLE, Département de Neurologie, Centre Mémoire de Recherche et de Ressources, Hôpital Gui de Chauliac, Centre Hospitalo-Universitaire de Montpellier
Les avancées dans le domaine du diagnostic de la maladie d’Alzheimer (MA) sont depuis quelques années majeures. En 2011, l’utilisation des biomarqueurs du LCR ainsi que de l’imagerie morphologique et fonctionnelle est possible en pratique clinique, et permet d’optimiser notre expertise diagnostique dans le champ des démences. Notre raisonnement clinique tient compte désormais d’examens complémentaires in vivo associés à la clinique et aux données neuropsychologiques. Ainsi, les profils atypiques ou différentiels de la MA bénéficient de ces avancées conceptuelles et technologiques.
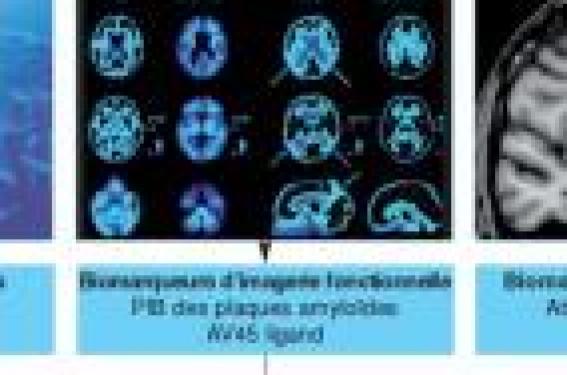
“To be or not to be a MA” en 2011 ? De nouveaux critères « diagnos t iques » de la maladie d’Alzheimer (MA) et de son stade précoce ont récemment été proposés (1,2). Ils intègrent aux données cliniques et neuropsychologiques les résultats des biomarqueurs in vivo d’imagerie fonctionnelle (TEP ou PIB) ou morphologique (IRM, volumétrie de l’hippocampe) et du liquide céphalorachidien (LCR) (dosages du peptide Aβ42, de la protéine Tau et de sa forme phosphorylée P-Tau) (figure 1). Grâce à ces biomarqueurs, il est possible de détecter un processus neurodégénératif de type Alzheimer in vivo très précocement. En pratique, l’utilisation de ces biomarqueurs modifie notre raisonnement clinique, surtout en cas de doute diagnostique. Avant ces marqueurs, la précision du diagnostic dépendait de notre expertise clinique, des données d’interrogatoire, des tests neuropsychologiques et du suivi. Actuellement, il dépend de notre accès aux différents plateaux techniques de biomarqueurs et de notre interprétation des résultats en fonction de notre expertise dans ces nouveaux domaines. Légendes : LCR : liquide céphalorachidien ; Aβ : peptide amyloïde ; P-Tau = Tau phosphorylée ; PIB : Pittsburg Compound B ; IRM : imagerie par résonnance magnétique. Figure 1. Représentation schématique des 3 types de biomarqueurs diagnostiques disponibles pour le diagnostic de la MA et de ses diagnostics différentiels. L’utilisation des biomarqueurs dans le liquide céphalorachidien et les marqueurs d’imagerie fonctionnelle de type marqueurs de plaques amyloïdes sont le reflet des processus neuropathologiques, des plaques séniles et des dégénérescences neurofibrillaires. Les marqueurs d’imagerie morphologique comme l’IRM nous donnent des informations sur la progression de la maladie. Grâce au développement des biomarqueurs de la MA, l’approche diagnostique de « to be or not to be a MA ? » se base sur une analyse combinée des résultats cliniques, neuropsychologiques, du LCR et de l’imagerie morphologique et fonctionnelle. Une analyse combinatoire étape par étape L’étape clinique Elle est essentielle pour évoquer les grands cadres nosologiques : mémoire, langage, comportement et autres troubles cognitifs. • Plainte de mémoire Il faut identifier le type de plainte mnésique : épisodique, sémantique, procédurale ; son caractère isolé ou associé à d’autres déficits cognitifs ; la rapidité de son apparition et celle du déclin cognitif. Tout déficit épisodique hippocampique à type d’oubli à mesure des événements de vie avec des difficultés pour les nouveaux apprentissages, un effet limité de l’indiçage et la présence d’intrusions, fait fortement évoquer une MA. Les profils différentiels sur une entrée mnésique font souvent état d’autres déficits cognitifs associés (sémantiques, dysexécutifs) ou une prédominance de troubles cognitifs non mnésiques (phasiques, praxiques, gnosiques). Dans le champ non dégénératif, d’autres diagnostics sont à évoquer mais ne seront pas détaillés ici (figure 2). Légendes : MA : maladie d’Alzheimer ; AVC : accident vasculaire cérébral ; A. Com Ant : artère communicante antérieure ; CO : monoxyde de carbone ; tb : troubles. Figure 2. Arbre décisionnel en fonction de la présence ou non d’un syndrome amnésique, de la nature des troubles de la mémoire. • Plainte centrée sur un trouble du langage Figure 3. Représentation schématique simplifiée des orientations diagnostiques devant une aphasie. Les troubles du langage de type aphasique (figure 3) peuvent faussement être pris par le patient ou son aidant comme un trouble mnésique du rappel du mot. En cas de prédominance de troubles du langage, deux diagnost ics di f férent iels doivent être recherchés : une aphasie non fluente primaire progressive et une démence sémantique. • La démence sémantique s’intègre dans les dégénérescences lobaires frontotemporales (DLFT) et se caractérise par une aphasie fluente (atteinte de la sémantique verbale) avec une perte du sens des mots en dénomination et compréhension, associée à une atteinte de la sémantique visuelle par une agnosie associative des objets (troubles de la reconnaissance de l’identité des objets) et des visages (troubles de la reconnaissance de l’identité des visages familiers). Le tableau associe une aphasie asémantique à une agnosie associative, à des paraphasies sémantiques, une dyslexie, une dysgraphie de surface, sans signes pariétaux ni d’agrammatisme. Un groupe de réflexion français propose de nouveaux critères intégrant les données cliniques, neuropsychologiques et l’imagerie pour définir des formes typiques et atypiques (tableau 1) (3). Toute atteinte des connaissances sémantiques isolée doit faire évoquer une DS. • L’aphasie non fluente progressive (ANFP). Bien qu’un symptôme aphasique puisse être présent dans un certain nombre d’affections neurodégénératives, le caractère inaugural et isolé doit faire évoquer une ANFP. Elle est regroupée dans les DLFT, mais un tiers d’entre elles sont des MA histolopathologiques (4). Cliniquement, un manque du mot, des erreurs phonétiques, un agrammatisme sont observés, alors que la compréhension est normale et les systèmes pariétaux préservés. Au cours des 2 premières années d’évolution, certains signes sont acceptés comme l’apraxie visuo-constructive, un syndrome dysexécutif et une agnosie associative sémantique pour les objets et/ou les visages ; alors que les systèmes épisodiques, visuo-perceptifs, visuo-spatiaux et comportementaux doivent être intègres. Plus de 30 % des ANFP cliniques sont des MA neuropathologiques. Tableau 1. Critères diagnostiques de la démence sémantique proposés par un groupe de réflexion français sous l’égide du Dr Moreaud. 1. On peut retenir le diagnostic de démence sémantique typique chez un patient présentant les critères 1.1 à 1.3 : • 1.1 - Perte des connaissances sémantiques attestée à la fois par : - un manque du mot pour les objets et/ou les personnes, un trouble de la compréhension des mots, un déficit de l’identification des objets et/ou personnes ; - portant autant que possible sur les mêmes objets et/ou personnes ; - s’installant insidieusement et s’aggravant progressivement. • 1.2 - En l’absence : - de troubles perceptifs, attestés par la normalité de la copie de dessins, la normalité des performances dans les tâches perceptives ; - de déficit de mémoire au jour le jour (un déficit dans les tests de mémoire n’exclut pas le diagnostic) et de désorientation temporelle ; - de réduction de la fluidité du discours ; - d’altération des composantes phonologiques (arthriques et phonémiques, attestée par la normalité de la répétition des mots, de la lecture et de l’écriture des mots réguliers) et syntaxiques du langage ; - d’altération du raisonnement non verbal, orientation spatiale, imitation de gestes, capacités visuo-spatiales, calcul ; un déficit dans les tâches exécutives n’exclut pas le diagnostic ; - d’anomalies de l’examen neurologique et de perte d’autonomie en dehors de celle générée par les troubles sémantiques. • 1.3 - Avec anomalies temporales habituellement bilatérales et asymétriques visualisées à l’imagerie morphologique (atrophie à l’IRM si possible) et/ou fonctionnelle (hypométabolisme au SPECT). 2. La démence sémantique est atypique s’il existe : • 2.1 - Un déficit unimodal progressif attesté par : - soit un manque du mot pour les objets et/ou les personnes et un trouble de la compréhension des mêmes mots, sans déficit de l’identification des objets et/ou personnes (forme verbale) ; - soit un manque du mot pour les objets et/ou les personnes avec déficit de l’identification des mêmes objets et/ou personnes, sans troubles de la compréhension des mots (forme visuelle). - si les critères 1.2 et 1.3 sont respectés. • 2.2 - La présence au cours de l’évolution d’un des signes suivants, s’il reste discret et au second plan : - troubles perceptifs ; - anomalies de la mémoire au jour le jour ; - anomalies de la lecture et de l’écriture des mots réguliers ; - altération du raisonnement non verbal, orientation spatiale, imitation de gestes, capacités visuo-spatiales, calcul ; - anomalies de l’examen neurologique ni perte d’autonomie dépassant celle générée par les troubles sémantiques ; - si les critères 1.1 et 1.3 sont respectés. 3. Sont en faveur du diagnostic de démence sémantique mais non indispensables : - des modifications de la personnalité et du comportement, comme : égocentrisme, idées fixes, rigidité mentale, diminution du répertoire comportemental, modifications des goûts et habitudes (par exemple : religiosité, changement de goût alimentaire), parcimonie, perte de la notion de danger ; - la présence dans le discours de paraphasies sémantiques ; - une réduction de la fluence catégorielle plus marquée que l’atteinte de la fluence formelle ; - une dyslexie et dysorthographie de surface. 4. Le diagnostic de démence sémantique est exclu, si : - l’IRM met en évidence une lésion non dégénérative permettant à elle seule d’expliquer le tableau clinique (exemple : AVC, tumeur) ; - un syndrome amnésique ou des troubles du comportement sont inauguraux et restent au premier plan ; - il existe une aphasie sans trouble de la compréhension des mots et de l’identification des images. • Une plainte mnésique révélant des troubles dysexécutifs cognitifs et comportementaux. Le Groupe de réflexion sur l'évaluation des fonctions exécutives (GREFEX), sous l’égide du Pr Godefroy, a récemment publié (5) de nouveaux critères et outils diagnostiques pour les troubles dysexécutifs (tableau 2). Ces outils permettent d’optimiser le diagnostic de ces troubles qui sont particulièrement fréquents dans la MA (apathie 60 %, anosognosie 65 %, troubles du shifting mental 45 %), mais qui orientent principalement vers des signes précoces de démence frontotemporale comportementale (fv-DFT) après exclusion des pathologies psychiatriques (dépression, état maniaque, troubles obsessionnels compulsifs). De nouveaux critères diagnostiques des troubles dysexécutifs cognitifs et comportementaux sont proposés par le GREFEX. Les troubles dysexécutifs sont fréquents et précoces dans la MA,mais orientent en premier lieu vers une démence frontotemporale comportementale (vf-DFT). • D’autres atteintes cognitives peuvent prédominer. • L’atteinte gnosique : des signes d’atrophie corticale postérieure (ACP ou syndrome de Benson) doivent être recherchés. Bien que les lésions neuropathologiques de l’ACP soient majoritairement de type MA, les signes cliniques font écho à une MA atypique et s’intègrent parfois dans les diagnostics différentiels. Le tableau clinique associe une agnosie visuelle associative, une désorientation topographique, une simultagnosie, une alexie, une agraphie spatiale, un syndrome de Gerstmann, une ataxie optique, puis un syndrome de Balint complet, une extinction visuelle, voire un déficit campimétrique en quadrant ou en hémichamp. Des apraxies constructives, de l'habillage, idéomotrice, une dysorthographie et une acalculie sont parfois observées. Une prédominance de troubles visuo-spatiaux orientent vers une maladie à corps de Lewy, il convient alors de rechercher des hallucinations visuelles, un syndrome extrapyramidal, des chutes précoces. • L’atteinte praxique : une dégénérescence cortico-basale doit alors être évoquée en recherchant des signes extrapyramidaux (rigidité, bradykinésie, dystonie, tremblement), des troubles de la sensibilité corticale et un « alien limb ». • Ne pas méconnaître une maladie de Creutzfeldt- Jakob (CDJ) devant un déclin rapide. En particulier, pour le diagnostic de nouveaux variants dont le tableau clinique se caractérise par des troubles cognitifs rapidement progressifs et létaux (médiane : 14 mois [6-39]) (Heath et coll. 2010) ; la présence de signes sensitifs douloureux peut aider au diagnostic. L’apport des biomarqueurs pour les diagnostics différentiels • L’analyse du profil des biomarqueurs du LCR Le profil typique MA des biomarqueurs du LCR associe une diminution du peptide Aβ42 (< 400 pg/ml) et une augmentation du taux de Tau totale (> 450 pg/ml) et de sa forme phosphorylée P-Tau (> 60 pg/ ml). Ce profil argumente en faveur d’un processus Alzheimer in vivo. En cas d’atypie clinique mais de profil typique de la MA, la sensibilité et la spécificité du diagnostic sont supérieures à 90 %. La HAS (2008) recommande leur réalisation en cas de profil atypique et chez le sujet jeune. L’apport des biomarqueurs du LCR dans la discrimination des diagnostics différentiels de MA, vf-DFT, DS ou maladie à corps de Lewy (DCL), est majeur (tableau 3). Récemment, certains ratios ou biomarqueurs ont été proposés pour discriminer les sujets MA des vf-DFT, DS ou DCL. Ainsi, le ratio P-Tau/Aβ42 permet de discriminer les sujets MA des DFT avec une sensibilité/spécificité (Se/Sp) de 91/98 % et les MA des DS avec une Se/Sp de 92,6/84,2 % (6). Les dosages du peptide Aβ38 (7,8) et du sAPPβ (8) sont également pertinents dans l’arsenal diagnostique MA versus vf-DFT. Pour la discrimination MA vs DCL, le peptide Aβ40 et le ratio Aβ42/Aβ38 (Se/Sp : 78/67 %) sont intéressants (9) (Bibl et coll. 2007). Concernant les diagnostics différentiels de type ANFP ou ACP, le profil des queurs dans le LCR n’est pas si discriminant (les ratios T-Tau/ Aβ[42] et P-Tau/Aβ[42] étant altérés dans 60 % ANFP et 61 % ACP respectivement). Majoritairement, les ANFP ont un profil de type MA (10), profil également observé chez 90 % des ACP cliniques, corroborant les données neuropathologiques de ces affections4. Pour les DS, peu de données sont disponibles, mais il semblerait qu’un profil de type MA soit retrouvé dans un tiers des cas et de type DFT dans deux tiers des cas. Le dosage du peptide Aβ38 dans le LCR est intéressant pour discriminer les vf-DFT des MA, celui de l’Aβ40 semble pertinent pour différencier les MA des DCL. Les profils des ANFP et ACP correspondent majoritairement au pattern LCR typique d’une MA. • Selon le pattern d’hypoperfusion à la TEP cérébrale eβt/ou de fixation des traceurs amyloïdes, un hypométabolisme du cortex temporopariétal et cingulaire postérieur en TEP est caractéristique d’une MA. L’hypoperfusion temporopariétale est également observée dans les tableaux cliniques de DLFT, mais induit souvent en erreur. L’atteinte des régions temporales antérieures et cingulaires antérieures est plus spécifique d’une DLFT (11). Un profil d’hypoperfusion prédominant en occipital évoque principalement une DCL, un hypermétabolisme en 18F-FDG-TEP au niveau des ganglions de la base, du cervelet et de l’aire prémotrice a récemment été observé (12). Pour les diagnostics différentiels, les données de 18F-FDG-TEP sont comparables à celles du marqueur spécifique du peptide β-amyloïde (TEP-11C-PIB) (13). Une fixation du PIB en frontal, pariétal, temporal latéral et cingulaire postérieur est objectivée dans la MA. Pour discriminer une MA vs DLFT, les zones les plus discriminantes sont le pôle temporal et le néocortex temporal (14). Dans les DCL, la fixation du traceur est prédominante dans les aires associatives, le cingulum et le striatum. La charge amyloïde dans la DCL est associée au profil de déclin (15). L’écueil majeur de cette technique reste sa non-réalisation en pratique clinique de routine. • Selon la localisation et le degré d’atrophie cérébrale et hippocampique. En pratique, l’imagerie morphologique permet d’éliminer les pathologies tumorales, inflammatoires, infectieuses, les lésions vasculaires et d’apprécier la localisation de l’atrophie corticale orientant le diagnostic. Dans la MA, l’atrophie touche le lobe temporal médial (amygdale, cortex entorhinal, périrhinal et parahippocampique), le gyrus cingulaire postérieur et le cortex temporo-pariétal. L’analyse du volume de l’hippocampe permet également d’opt imi ser le diagnostic et de caractériser la progression de la MA. Pour les DLFT, l’atrophie corticale s’étend en frontal, temporal antérieur, frontotemporale, contrairement aux DCL où l’atrophie prédomine en occipital. Mais bien souvent les patterns d’atrophie se chevauchent ou l’atrophie étant déjà globale, cela n’oriente plus le diagnostic. En recherche, les méthodes d’analyse évoluent considérablement (VBM, VBMDARTEL, SVM [Support vector machine]) dans le but d’analyser des volumes corticaux, l’extension lésionnelle, le degré d’asymétrie. La validation de ces outils et leur accessibilité ultérieure permettra d’optimiser notre pertinence clinique. De plus, l’avenir semble à la combinaison des techniques. Ainsi, les données combinées PET-FDG et IRM permettraient une exactitude diagnostique « MA vsDLFT » de 94 % (16). En pratique Le raisonnement « diagnostic » clinique dans le domaine des maladies neurodégénératives est en pleine mutation. Les avancées dans le domaine des biomarqueurs de la maladie d’Alzheimer ouvrent de nouveaux champs diagnostiques in vivo pour les affections apparentées (diagnostics différentiels). Nos diagnostics dans le domaine des démences se fondent désormais sur la combinaison plus ou moins complète, en fonction de l’accès aux plateaux techniques, des résultats des biomarqueurs du LCR, et de ceux de l’imagerie morphologique et fonctionnelle. La validation de ces biomarqueurs et la découverte de nouveaux permettra d’optimiser nos connaissances et notre prise en charge des patients et de leur famille.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :