Publié le 26 nov 2009Lecture 20 min
Place de l’imagerie neurologique dans la prise en charge du patient traumatisé crânien grave
T. LESCOT, L. ABDENNOUR, L. PUYBASSET, Réanimation Neurochirurgicale, Département d’Anesthésie – Réanimation, Pitié-Salpêtrière ; Université Pierre et Marie Curie, Paris
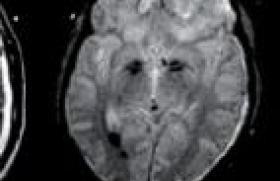
Les avancées technologiques de l’imageriemédicale ces 30 dernières années ont bouleversé la prise en charge des patients traumatisés crâniens graves. Depuis son développement, le scanner cérébral s’est imposé comme l’examen de choix à réaliser à la phase aiguë. Sa généralisation a permis de faire progresser nos connaissances physiopathologiques, d’élaborer une prise en charge rationnelle, et ainsi d’améliorer le pronostic des patients victimes de traumatisme crânien grave (score de Glasgowinitial inférieur à 8). L’imagerie par résonance magnétique (IRM) beaucoup plus sensible et bien plus précise permet d’établir un bilan exhaustif des lésions cérébrales, et représente une aide précieuse dans l’évaluation du pronostic de ces patients. Le couplage de séquencesmorphologiques à des séquences d’évaluationsmétaboliques ouvre une perspective de recherche particulièrement intéressante. Néanmoins, la durée des différentes séquences nécessaires à sa réalisation, ainsi que l’environnement particulier dans lequel est effectué cet examen, expliquent que l’IRMn’est le plus souvent envisagée qu’à distance du traumatisme.
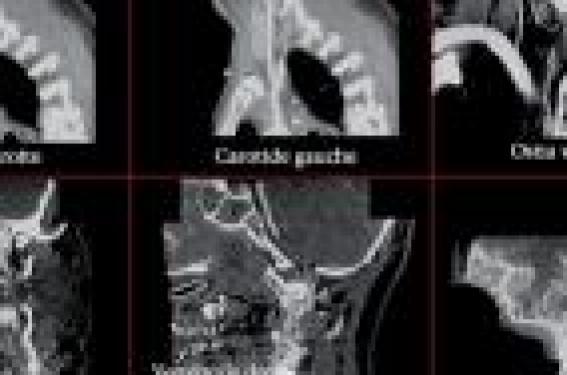
Scanner cérébral Indications Le scanner cérébral représente l’examen de choix à réaliser en première intention après un traumatisme crânien, et doit systématiquement être effectué en urgence en cas de score de Glasgow inférieur à 15, de présence d’une fracture du crâne, de crise convulsive, de signes cliniques évoquant une fracture de la base du crâne, de signes neurologiques de localisation ou de céphalées persistantes (1). La grande disponibilité de cette technique, la rapidité de son acquisition, sa reproductibilité et son coût modéré expliquent la place conquise par la tomodensitométrie dans l’évaluation du patient traumatisé crânien. Le scanner cérébral permet, dans ce contexte, la détection d’un hématome intra- ou extraparenchymateux, d’un oedème cérébral, d’une contusion cérébrale, d’un effet de masse ou d’une pneumencéphalie. Chez les patients les plus graves, sa réalisation doit être la plus rapide possible, afin d’évaluer la nécessité d’une intervention chirurgicale ou d’unmonitorage de la pression intracrânienne. Le développement et la diffusion récente de scanner «multibarrettes » offrent la possibilité d’étendre le champ d’exploration aux structures osseuses (recherche d’une fracture du rachis cervical) et vasculaires (recherche d’une dissection des vaisseaux du cou ou d’une dissection intracrânienne) en un temps restreint (figure 1) Une attention toute particulière doit être apportée aux explorations scanographiques effectuées très précocement (dans les 3 premières heures suivant un traumatisme crânien grave) ; une imagerie normale à ce stade n’exclut pas la survenue ultérieure de lésions cérébrales (2) et en particulier la constitution retardée d’un hématome extradural après un intervalle libre de quelques heures ou l’aggravation majeure d’une contusion cérébrale (figure 2). Figure 1. Angioscanner des vaisseaux du cou : examen normal. Figure 2. Évolution temporelle d’une contusion hémorragique frontale droite. A: tomodensitométrie cérébrale réalisée 2 heures après le traumatisme. B : tomodensitométrie cérébrale réalisée 16 heures après le traumatisme chez lemême patient après dégradation du score de Glasgow. Imagerie par résonance magnétique Indications Contrairement au scanner, l’IRM n’est que très rarement un examen à faire en urgence chez le patient traumatisé crânien grave. De réalisation délicate et potentiellement dangereuse chez un patient instable, il apporte en revanche de précieuses informations dans le bilan lésionnel à distance de la phase aiguë, et est le plus souvent pratiqué à partir de la deuxième semaine en cas de mauvaise évolution clinique persistante. Le couplage de séquences morphologiques à des séquences de diffusion et de spectroscopie permet une description précise de la nature et de la localisation des lésions. Contrairement au scanner, l’IRM n’est que très rarement un examen à faire en urgence. Précautions Le champ magnétique est toujours présent dans l’environnement de l’appareil d’IRM, même quand celui-ci n’acquiert pas de séquence. De ce fait, il existe un réel risque « d’effet projectile » si des objets ferromagnétiques tels qu’un obus d’oxygène, un moniteur de surveillance ou un respirateur de transport pénètrent dans la pièce dédiée à l’IRM. Aujourd’hui, plusieurs appareils dédiés non ferromagnétiques sont disponibles sur le marché dont des respirateurs d’anesthésie à circuit fermé. Le monitorage se fait à l’aide d’un matériel adapté non ferromagnétique, préinstallé dans la pièce. L’électrocardiogramme, la SpO2, la pression artérielle invasive ou non invasive, ainsi que l’EtCO2 doivent être mesurés lors de l’examen. L’utilisation de seringues électriques (sédation, catécholamines) est possible. Celles-ci doivent alors être positionnées à distance de l’appareil d’IRM. Des rallonges de grande taille sont à prévoir avant le transport du patient. Il n’existe pas aujourd’hui de seringues électriques dédiées à l’IRM. Dans l’état actuel du matériel disponible, la vitesse d’administration des drogues peut être influencée par le champ magnétique : il existe donc un risque d’instabilité hémodynamique chez les patients dépendants de la régularité de l’administration de catécholamines. Enfin, la surveillance clinique et l’accès au patient sont rendus difficiles pendant l’examen IRM, car celui-ci est positionné assez loin dans l’appareil. La présence d’instruments ferromagnétiques, de type pacemaker, pompe implantable ou neurostimulateur, est une contre-indication formelle à la réalisation d’une IRM. Il existe un risque de déplacement, de réchauffement ou de dérèglement de l’instrument. Lorsqu’une valve cardiaque ou un clip sont présents, il est préalablement nécessaire de s’assurer de leur caractère non ferromagnétique. Les coils récents ne sont pas ferromagnétiques : ils ne contreindiquent donc pas l’examen. La présence d’un capteur de pression intraparenchymateux est responsable d’artefacts de mesure. Le réglage des valves internes de dérivation ventriculaire peut être modifié après la réalisation d’une IRM. Le plus souvent, la valve se positionne en haute pression de dérivation. Cette hypothèse doit être systématiquement évoquée devant l’apparition d’une aggravation neurologique au décours de la réalisation d’une IRM chez un patient porteur d’un tel dispositif. Il est ainsi recommandé d’effectuer un contrôle radiologique du réglage de la valve de dérivation avant et après l’examen. Séquences morphologiques Les séquences morphologiques habituellement réalisées dans le bilan du patient traumatisé crânien grave comprennent les séquences pondérées en T1, T2 et T2* et FLAIR (Fluid Attenuated Inversion Recovery). Cette dernière représente une technique d’acquisition permettant d'obtenir des images très fortement pondérées en T2 tout en supprimant le signal des liquides, tels que le LCR. Cette séquence est supérieure au T2 pour détecter l’oedème cérébral et mettre en évidence des lésions situées à proximité des ventricules. Angiographie par résonance magnétique (ARM) Ne nécessitant pas l’injection de produit de contraste, l’ARM est intéressante en traumatologie, pour infirmer ou affirmer l’existence d’une dissection vasculaire traumatique qui nécessitera la mise sous anticoagulants à dose efficace en l’absence de contreindications. Séquences de diffusion et tenseur de diffusion Le phénomène de diffusion moléculaire correspond aux mouvements aléatoires de translation des molécules, appelés mouvements browniens. Contrairement à la diffusion de l’eau dans un liquide où lesmolécules d’eau se déplacent de façon isotrope sans rencontrer d’obstacle, la mobilité des molécules d’eau dans les tissus biologiques est influencée par la structure tissulaire. Les différents composants tissulaires (la membrane cytoplasmique, le cytosquelette, la myéline) constituent des obstacles physiques qui entravent la mobilité des molécules d’eau. L’interaction desmolécules d’eau avec les constituants tissulaires se traduit alors par une réduction du coefficient de diffusion de l’eau. L'intérêt essentiel de cette séquence est que seul un nombre très limité de pathologies entraînent une diminution de ce paramètre. Il s'agit en particulier des abcès et de l'ischémie à la phase aiguë. L’imagerie de tenseur de diffusion cherche à déterminer si la « diffusibilité » de l'eau s'exerce dans une direction préférentielle (anisotrope). Ceci se produit dans les faisceaux de fibres blanches, où l'eau, canalisée par les membranes, ne peut se déplacer que dans le sens des axones ou des dendrites. Cette séquence permet donc de déterminer si ces structures sont intactes ou détruites. Moins largement disponible que la séquence d’imagerie de diffusion, elle permet une bien meilleure analyse de l’état de la substance blanche, en particulier pour la détection des lésions axonales diffuses ou des conséquences de l’hypertension intracrânienne. L’IRM spectroscopique La spectroscopie par résonance magnétique permet une évaluation non invasive de substances biochimiques intracellulaires, c’est-à-dire de quantifier la concentration en créatine (Cr), choline (Cho) et N-acétyl-aspartate (NAA) d’une région donnée du parenchyme (spectroscopie monovoxel) ou bien d’une section de coupe IRM (analyse multivoxel). La spectroscopie repose sur l’étude de la fréquence de résonances des spins des atomes. Pour un atome donné correspond une fréquence de résonance du spin qui est fonction de l’espèce biochimique dans laquelle se trouve cet atome. Grâce à une application mathématique, on obtient le spectre des fréquences pour un atome. L’application de la spectroscopie par résonance magnétique à l’encéphale permet l’étude du spectre de résonance de l’atome d’hydrogène H1 ou de l’atome de phosphore P31. L’analyse du spectre des fréquences de résonance de l’atome d’hydrogène met en évidence un certain nombre de pics correspondant aux molécules de N-acéthylaspartate (NAA), de créatine (Cr) et de choline (Cho). Le ratio NAA/créatine serait un marqueur indirect de l’activité neuronale, alors que le ratio choline/ créatine serait un marqueur indirect de l’activité gliale. Apport de l’imagerie dans la décision chirurgicale Dans le cadre du traumatisme crânien grave, la première question à laquelle l’imagerie précoce doit répondre est celle de l’existence d’une urgence neurochirurgicale. L’équipe médicochirurgicale doit confronter les conditions de survenue du traumatisme et l’état clinique du patient aux données scanographiques. À la phase aiguë, les urgences neurochirurgicales traumatiques sont dominées par les hématomes extra- et sousduraux, avec déviations de la ligne médiane et par les embarrures ouvertes ou parfois fermées. Dans en second temps, les contusions temporales avec disparition de la citerne et anisocorie homolatérale (figure 3), les contusions frontales avec hypertension intracrânienne incontrôlable et l’existence d’un oedème massif avec hypertension intracrânienne incontrôlable peuvent faire l’objet d’un traitement chirurgical. Apport de l’imagerie dans le bilan lésionnel Lésions extraparenchymateuses Hématome extradural L’hématome extradural résulte de la constitution d’une collection sanguine comprise entre la boîte crânienne et la dure-mère, et est le plus souvent associé à une fracture du crâne en regard. Il est la conséquence d’une lésion d’une artère ou veine méningée, plus rarement de la rupture d’un sinus veineux. Son diagnostic est scanographique, et sa présentation est celle d’une lentille biconvexe, spontanément hyperdense, bien limitée, accompagnée d’un effet demasse sur le parenchyme adjacent. Figure 3. Volumineuse contusion hémorragique temporale droite avant (A) et après (B) évacuation chirurgicale. En cas de constitution très récente et/ou très rapide, son aspect peut-être celui d’une collection hétérogène avec coexistence de plages hypo- et hyperdenses traduisant l’existence de sang collecté et de sang encore liquide. La possibilité d’une apparition retardée de cette lésion impose une interprétation prudente des images et le renouvellement de l’examen lorsque la réalisation de celui-ci est précoce. Hématome sous-dural Résultant de lésions de petites veines traversant l’espace sousarachnoïdien, l’hématome sousdural se constitue entre l’arachnoïde et la dure-mère. Cette collection se situe le plus souvent au niveau de la grande convexité de la boîte crânienne. L’association d’un hématome sous-dural et d’une contusion parenchymateuse sous-jacente est fréquente, rendant son pronostic plus sévère que celui des hématomes extraduraux à volume égal. Son diagnostic repose sur la réalisation d’un scanner cérébral sans injection de produit de contraste révélant une lame hyperdense homogène étalée en croissant à limite interne concave. L’association d’un hématome sous-dural et d’une contusion parenchymateuse sousjacente est fréquente. Hémorragieméningée La représentation scanographique de l’hémorragie méningée est celle d’une hyperdensité spontanée homogène des espaces sous-arachnoïdiens. Elle est retrouvée dans environ 35%des cas de traumatismes crâniens, et constitue un facteur indépendant de mauvais pronostic (3). Hématome intraventriculaire La présence de sang au sein du système ventriculaire se traduit par une hyperdensité spontanée au sein du liquide céphalorachidien ventriculaire. Souvent secondaire à l’extension d’une contusion hémorragique, l’hémorragie ventriculaire est rare et expose au risque d’hydrocéphalie par blocage des voies d’écoulement du LCR. Pneumencéphalie Une pneumencéphalie est suspectée devant la présence de bulles d’air hypodenses au sein de la boîte crânienne. Elle traduit l’existence d’une fracture de la base du crâne impliquant un sinus, ou d’une brèche duremérienne associée à une fracture ouverte. Dissection vasculaire La présence d’une lésion ischémique systématisée dans un territoire artériel doit faire évoquer l’existence d’une dissection vasculaire. Celle-ci peut intéresser une artère carotide dans sa portion extra- ou intracrânienne ou bien une artère vertébrale. Sa mise en évidence repose sur la réalisation d’une angiographie des vaisseaux du cou par une technique tomodensitométrique, d’imagerie par résonance magnétique ou de radiologie conventionnelle. La recherche d’une dissection vasculaire doit être systématique en cas de fracture de la base du crâne associée à un traumatisme crânien grave. Elle est indispensable en cas de lésion cervicale associée (fracture du rachis, contusion des parties molles). La recherche d’une dissection vasculaire doit être systématique en cas de fracture de la base du crâne associée à un traumatisme crânien grave. Lésions intraparenchymateuses primaires OEdème cérébral L’oedème cérébral post-traumatique se développe dans les heures et jours suivant le traumatisme. Qu’il soit vasogénique ou ischémique (cytotoxique), il expose au risque de déplacement et d’engagement des structures cérébrales, d’hypertension intracrânienne, d’hypoperfusion cérébrale et d’ischémie. Sa présentation scanographique associe une disparition des citernes de la base, une diminution de la taille des ventricules, une disparition des sillons corticaux et une dédifférenciation corticosous- corticale. Contusions hémorragiques Les contusions hémorragiques représentent des zones de destruction cérébrale résultant du choc direct de l’encéphale contre des zones saillantes de la structure osseuse de la boîte crânienne. Pour cette raison, elles se constituent le plus souvent au niveau des lobes frontaux et temporaux. Elles sont le plus souvent associées à des lésions de contrecoup. Les contusions hémorragiques sont constituées d’un noyau central hémorragique, hyperdense, entouré d’une zone de tissu cérébral hypoperfusé à risque ischémique, hypodense. Dans les heures et jours suivant le traumatisme, se forme un halo oedémateux péricontusionnel de mécanisme ischémique (cytotoxique) et vasogénique. Au sein des contusions, la destruction du parenchyme cérébral s’accompagne d’une augmentation accrue de la perméabilité de la barrière hémato-encéphalique, notamment au produit de contraste (4,5). Dans ces conditions, l’utilisation agressive de thérapeutiques osmotiquement actives doit être réfléchie en cas de zones contuses étendues (6). La présentation de ces contusions en imagerie est variable en fonction des patients, du traumatisme et du temps. Lésions axonales diffuses Les forces d’accélération-décélération et de rotation appliquées à la boîte crânienne lors du traumatisme se traduisent par des lésions de cisaillements des fibres nerveuses. Figure 4. Lésions axonales diffuses hémorragiques du corps calleux, visibles sous la forme d’hyposignaux en séquences pondérées T2* après accident de la voie publique. Le patient a présenté une bonne évolution clinique dans les suites. Figure 5. Lésions axonales diffuses non hémorragiques du corps calleux. Aucune anomalie n’est détectée au scanner (A). Il existe un hypersignal en FLAIR (B). La séquence en T2* n’objective pas d’hémorragie (C). L’hypersignal est trèsmarqué en diffusion (D). Ces lésions de la substance blanche, appelées lésions axonales diffuses, sont localisées aux zones de jonction de tissus de densités différentes. Elles peuvent êtres hémorragiques ou ischémiques. Elles siégent préférentiellement à la jonction entre la substance grise et la substance blanche des lobes frontaux et temporaux, au niveau du corps calleux, des ganglions de la base et du tronc cérébral. À la phase aiguë, la tomodensitométrie peut révéler la présence de lésions axonales diffuses sous la forme de petites pétéchies punctiformes. Néanmoins, le scanner cérébral est peu sensible. De plus, il sousestime la quantité et la taille de ces lésions. L’IRM permet de détecter les lésions axonales diffuses et doit être réalisée chez tous les patients présentant peu de lésions au scanner cérébral contrastant avec un coma profond. Les lésions axonales diffuses de type hémorragique, non détectées par le scanner cérébral, sont visibles sur les séquences en écho de gradient en pondération T2*. Elles apparaissent sous la forme d’un hyposignal et traduisent la présence de désoxyhémoglobine paramagnétique (figure 4). Le nombre de lésions en T2* et leur localisation seraient corrélés à la gravité clinique du patient et à son pronostic à moyen terme (7). L’IRM permet également de détecter des lésions axonales diffuses non hémorragiques (8). Celles-ci peuvent expliquer les troubles de la conscience observés après un traumatisme crânien malgré un aspect normal au scanner cérébral. Typiquement, il s’agit de lésions hyperdenses en FLAIR qui s’accompagnent d’hypersignaux en diffusion (diminution du coefficient de diffusion) sans anomalies en T2*(9). Ces lésions sont le plus souvent situées au niveau du corps calleux, des noyaux gris centraux, des pédoncules et de la protubérance (figure 5). L’IRM spectroscopique peut aider à la détection des lésions axonales diffuses. Les données de travaux expérimentaux (10) et cliniques (11-13) ontmis en évidence une diminution de NAA secondaire à une souffrance neuronale et une augmentation de choline témoignant d’une prolifération microgliale au sein de la substance blanche frontale, bien que celleci apparaisse normale sur les séquences morphologique. De plus, cette réduction de NAA était corrélée avec la sévérité du traumatisme (12) et était associée à un moins bon pronostic à 6 mois (13). Lésions intraparenchymateuses secondaires La constitution d’un hématome, l’aggravation d’unoedème cérébral dans l’enceinte close et inextensible de la boîte crânienne peuvent conduire des modifications des pressions intracrâniennes et se compliquer d’engagements cérébraux et de lésions ischémiques parfois secondairement hémorragiques. Les engagements cérébraux résultent de la compression de structures cérébrales par déplacements. On décrit quatre grands types d’engagements cérébraux : l’engagement sous la faux du cerveau, l’engagement transtentoriel, l’engagement par la fente de Bichat et l’engagement par le trou occipital. L’engagement sous la faux du cerveau ou engagement cingulaire résulte d’un déplacement latéral des structures cérébrales. L’engagement trans-tentoriel résulte d’un déplacement céphalo-caudal des hémisphères vers le bas. Il se traduit rapidement par une mydriase bilatérale. L’engagement par la fente de Bichat ou engagement temporal est latéral, et correspond au passage de l’uncus et de l’hippocampe dans la fente de Bichat, entre le bord libre de la tente du cervelet et le tronc cérébral ; il se traduit par une anisocorie, puis unemydriase homolatérale. Dans ces deux cas, l’engagement peut s’accompagner d’une compression de l’artère cérébrale postérieure à l’origine d’une cécité corticale ischémique (figure 6). L’engagement par le trou occipital est exceptionnel en traumatologie et ne se rencontre que dans les lésions de fosse postérieure. Conclusion Figure 6. Hypersignal en séquence IRM de diffusion traduisant unoedème cytotoxique : ischémie dans le territoire de l’artère cérébrale postérieure secondaire à des épisodes d’engagements centraux. Le scanner cérébral reste l’examen de choix à réaliser en urgence chez tout patient traumatisé crânien dont l’examen neurologique n’est pas normal. Il permet de porter une indication neurochirurgicale ou de préciser la nécessité d’une prise en charge spécialisée en réanimation. L’IRMmorphologique et l’IRM spectroscopique offrent aujourd’hui la possibilité d’établir un bilan exhaustif des lésions cérébrales des patients traumatisés crâniens sévères. Ceci devrait permettre dans un avenir proche de préciser leur pronostic en termes d’éveil, et d’informer leurs proches au moyen d’arguments plus précis et fiables que ceux apportés par le simple examen scanographique. Points essentiels • Le scanner cérébral représente l’examen de choix à réaliser en première intention après un traumatisme crânien et doit systématiquement être effectué en urgence en cas de score de Glasgow inférieur à 15. • Une attention toute particulière doit être apportée aux explorations scanographiques effectuées très précocement (dans les 3 premières heures suivant un traumatisme crânien grave). •Contrairement au scanner, l’IRM n’est que très rarement un examen à réaliser en urgence chez le patient traumatisé crânien grave.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :